氨的"逆袭":中南大学余正团队揭示肠道细菌促进肠道蠕动、改善便秘的新机制
 2026-02-25
2026-02-25
 5482
5482

iNature
肠能动性是肠神经系统的功能,包括兴奋性神经递质乙酰胆碱(ACh)的分泌。虽然肠道共生细菌是肠道生理的关键调节者,但微生物影响肠道蠕动和便秘的分子机制仍不清楚。
这项研究揭示了一种新机制:肠道细菌可以通过产生氨气,来提升结肠内的乙酰胆碱水平,从而正向调控肠道蠕动。这为理解肠道微生物如何影响肠道功能以及治疗便秘等肠道动力障碍提供了新的视角和靶点。

肠蠕动是肠神经系统(ENS)调节的反射。乙酰胆碱(ACh)在这一过程中起着关键的兴奋性神经递质的作用。ACh信号传导的失调与各种肠运动障碍密切相关。临床证据表明,慢性便秘患者结肠组织中的乙酰胆碱释放显著减少。外源性ACh补充有效地增强了肠能动性。因此,乙酰胆碱在维持生理性肠蠕动中起着重要作用。
除了内在的ENS调节,微生物生态失调被广泛认为是胃肠疾病的重要驱动因素。研究表明,微生物群减少扰乱了神经源性运动程序,延长了肠道传输时间。至关重要的是,成年无菌小鼠体内微生物群的重建恢复了肠道神经元的兴奋性,为微生物群在调节肠道神经活动和活动性方面的重要作用提供了有力的证据。然而,微生物直接和特异性调节ENS神经元活动和蠕动结果的详细分子机制仍然是该领域中未解决的科学问题。
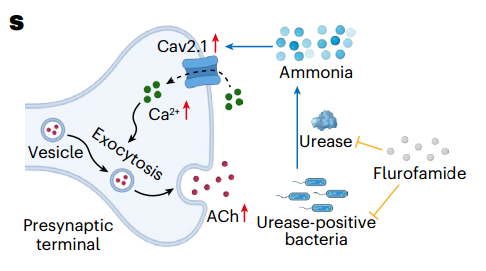
机理模式图(图源自Nature Microbiology)
在这里,研究人员报告了微生物氮代谢和通过氨产生的肠动力调节之间的联系。该研究在由ACh缺乏诱导的肠运动障碍小鼠模型和便秘患者中观察到肠氨水平和脲酶活性的代偿性升高。用从患者粪便中分离出的尿素酶阳性梭状芽孢杆菌或工程尿素酶表达细菌对小鼠进行氨补充或干预,可有效恢复结肠ACh水平。在体外,氨上调肠神经元上电压门控钙通道的表达,驱动Ca2+内流以增强ACh分泌。该研究揭示了一种微生物代偿机制,该机制对肠道中ACh水平的波动做出反应,并为肠道运动障碍提供了微生物靶点。