iNature
化疗是三阴性乳腺癌(TNBC)的主要治疗方法,但其疗效仍不令人满意。2025年7月21日,四川大学罗婷、敬静,徐州医科大学李世宝共同通讯在Signal Transduction and Targeted Therapy(IF=52.7)在线发表题为“Exploratory phase II trial of an anti-PD-1 antibody camrelizumab combined with a VEGFR-2 inhibitor apatinib and chemotherapy as a neoadjuvant therapy for triple-negative breast cancer (NeoPanDa03): efficacy, safety and biomarker analysis”的研究论文。该研究表明,卡瑞利珠单抗联合阿帕替尼联合化疗作为II-III期TNBC的新辅助治疗具有良好的临床疗效和安全性,值得进一步研究和临床应用。该研究是一项单臂、开放标签、单中心临床试验(NCT05447702),纳入华西医院新诊断的II-III期TNBC患者。治疗方案包括卡瑞利珠单抗(200mg,静脉注射,每2周一次,12个周期)、阿帕替尼(250 mg,口服,每日一次)和交替化疗[白蛋白结合型紫杉醇(d1、8、15,每4周一次)共4个周期以及表柔比星联合环磷酰胺(每2周一次)共4个周期]。从2023年6月至2024年4月,共入组35例患者,其中1例患者因不耐受不良反应退出。治疗完成后,总病理完全缓解(tpCR, ypT0/is, ypN0)率为67.6%(23/34),乳腺 pCR(ypT0/is)率为 70.6%(24/34)。新辅助治疗后的总有效率达到94.1%(32/34)。丙氨酸氨基转移酶(38.2%)和天冬氨酸氨基转移酶(29.4%)升高是最常见的3-4级不良事件,没有报告显著毒性或治疗相关死亡。通过Olink和RNA测序对新辅助治疗前后收集的血清和组织样本进行全面分析,发现该治疗诱导了复杂的全身免疫反应。这些发现促成了两个新型评分系统的开发:用于分层的治疗前反应预测评分系统和用于治疗反应评估的疗效评估评分系统。
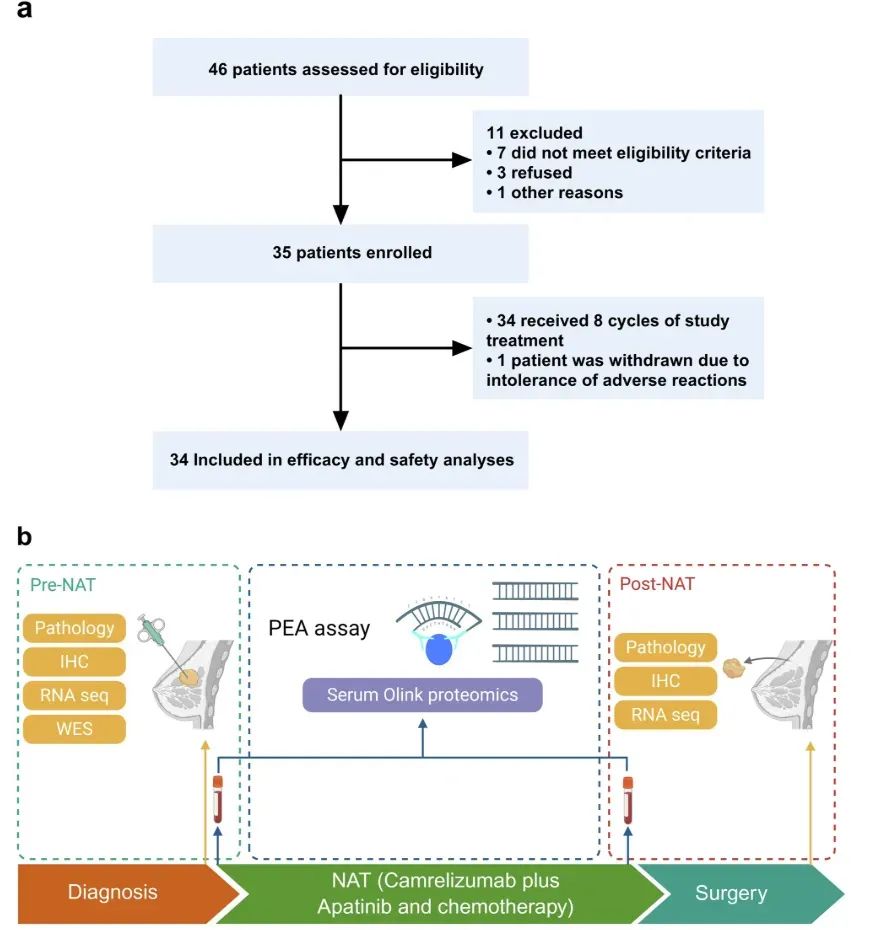
乳腺癌(BC)是全球女性最常见的恶性肿瘤,也是癌症相关死亡的主要原因。三阴性乳腺癌(TNBC)约占BC病例的15%,其定义是雌激素受体(ER)、孕激素受体(PR)和人表皮生长因子受体2(HER2)表达缺失。与其他分子亚型相比,这种侵袭性亚型具有独特的临床特征,包括疾病进展加速、早期复发模式和生存期较短。由于TNBC固有的生物学异质性以及缺乏已确定的分子靶点,其治疗前景仍然极具挑战性,导致其预后数十年来持续不佳。目前的标准治疗主要依赖于细胞毒性化疗,尽管最近的模式转变已将治疗重点从术后辅助方案转变为术前新辅助治疗。包括KEYNOTE-522在内的里程碑式临床试验的新证据进一步彻底改变了治疗方案,证明PD-1/PD-L1免疫检查点抑制剂(ICI)联合化疗在早期高危TNBC中具有更优的疗效。然而,对III期试验数据(GeparNuevo、IMpassion031、KEYNOTE-522)的关键分析揭示了持续存在的局限性,病理完全缓解(pCR)率稳定在 53.4-64.8%,近一半的患者未达到病理完全缓解(非pCR)。CamRelief试验确立了人源化抗PD-1单克隆抗体卡瑞利珠单抗联合化疗作为早期或局部晚期TNBC新辅助治疗(NAT)的临床可行性。该研究纳入了所有淋巴结状态的患者,包括N3期患者,并采用了强化化疗方案,方案包括白蛋白结合型紫杉醇联合卡铂,随后进行剂量密集型表柔比星联合环磷酰胺。结果显示,卡瑞利珠单抗联合化疗组的病理完全缓解率显著高于安慰剂联合化疗组(56.8% vs.44.7%)。值得注意的是,在III期患者中,卡瑞利珠单抗联合卡铂化疗组的病理完全缓解率为49.4%,而单纯化疗组为49.4%。这些比率超过了IMpassion031试验报告的数值(分别为45%和23%),进一步凸显了卡瑞利珠单抗强大的抗肿瘤活性。尽管如此,卡瑞利珠单抗化疗组中仍有2名患者(0.9%)发生了致命不良事件。因此,这些发现强调了迫切需要创新的组合策略来提高免疫治疗效果。越来越多的临床前和临床证据支持抗血管生成药物在增强免疫检查点阻断方面具有协同潜力。从机制上讲,抑制血管内皮生长因子(VEGF)通路可通过促进免疫细胞浸润、激活T细胞和调节PD-1/PD-L1来重塑肿瘤微环境。这一科学原理已转化为临床成功,联合方案已证明可改善晚期三阴性乳腺癌(TNBC)患者的生存结局。一项开放标签II期试验(NCT03394287)表明,阿帕替尼(一种口服生物可利用的酪氨酸激酶抑制剂,可选择性靶向血管内皮生长因子受体2(VEGFR-2))与卡瑞利珠单抗联合治疗在晚期三阴性乳腺癌患者中获得了良好的ORR和PFS,无论既往治疗方案或PD-L1状态如何。无化疗方案的ORR达到43.3%,显著高于抗PD-1/PD-L1抗体单药治疗(5.2%-18.5%)或阿帕替尼单药治疗(10.7%)。这些结果凸显了联合治疗的良好临床疗效和可接受的安全性。尽管取得了这些进展,但仍存在关键的知识缺口。值得注意的是,KEYNOTE-522试验证明了PD-L1表达在预测新辅助免疫治疗获益方面的独立性,凸显了新型预测性生物标志物的重要性。此外,患者间治疗反应的巨大异质性需要精准医疗方法来优化治疗选择。为了应对这些挑战,研究团队设计了这项单组II期试验,研究卡瑞利珠单抗联合阿帕替尼和化疗的新辅助治疗在早期或局部晚期TNBC中的应用。根据 REMARK 肿瘤标志物预后研究指南,研究团队的研究纳入了前瞻性的肿瘤组织和外周血样本采集。通过全面的多组学分析,研究团队的目标是:(1)评估该方案的疗效和安全性;(2)识别预测治疗反应的生物标志物;(3)寻找针对非 pCRTNBC患者的潜在疗效增强策略,即卡瑞利珠单抗联合阿帕替尼和化疗。图1 研究设计和样本收集的流程图(图源自Signal Transduction and Targeted Therapy)
https://www.nature.com/articles/s41392-025-02337-1
 2025-07-23
2025-07-23
 7292
7292